Proceso isentrópico
En termodinámica, un proceso isoentrópico, a veces llamado proceso isentrópico (combinación de la palabra griega "iso" - igual - y "entropía"), es aquel en el que la entropía del sistema permanece constante.
Según la segunda ley de la termodinámica, se puede decir:
donde es la cantidad de energía que el sistema gana por transferencia de calor, es la temperatura de la fuente térmica que interviene en el proceso (si el proceso es reversible la temperatura de la fuente térmica será igual a la del sistema), y es el cambio en la entropía del sistema en dicho proceso. El símbolo de igualdad implicaría un proceso reversible. En un proceso adiabático reversible no hay transferencia de calor , y por tanto el proceso es isoentrópico. En un proceso adiabático irreversible, la entropía se incrementará, de modo que es necesario eliminar el calor del sistema (mediante refrigeración) para mantener una entropía constante. Por lo tanto, un proceso adiabático irreversible no es isoentrópico.[1][2][3][4][5][6] Las transferencias de trabajo del sistema son sin fricción, y no hay transferencia neta de calor o materia. Este proceso idealizado es útil en ingeniería como modelo y base de comparación para los procesos reales.[7]
Para procesos reversibles, una transformación isoentrópica se realiza mediante el aislamiento térmico del sistema respecto a su entorno. (proceso adiabático).
La temperatura es la variable termodinámica conjugada de la entropía, de modo que el proceso conjugado será isotérmico, y el sistema estará termicamente conectado a un baño caliente de temperatura constante. Los procesos isotérmicos no son isoentrópicos.
La palabra "isentrópico" puede interpretarse de otra manera, ya que su significado se deduce de su etimología. Significa un proceso en el que la entropía del sistema permanece inalterada; como se ha mencionado, esto podría ocurrir si el proceso es adiabático y reversible. Sin embargo, esto también podría ocurrir en un sistema en el que el trabajo realizado en el sistema incluye la fricción interna al sistema, y el calor se retira del sistema en la cantidad justa para compensar la fricción interna, a fin de dejar la entropía sin cambios.[8] Sin embargo, en relación con el universo, la entropía del mismo aumentaría como resultado, de acuerdo con la Segunda Ley de la Termodinámica.
Antecedentes[editar]
La segunda ley de la termodinámica establece[9][10] que
donde es la cantidad de energía que gana el sistema por calentamiento, es la temperatura del entorno, y es el cambio de entropía. El signo de igualdad se refiere a un proceso reversible, que es un límite teórico idealizado imaginado, que nunca se da en la realidad física, con temperaturas esencialmente iguales del sistema y del entorno.[11][12] Para un proceso isentrópico, si también es reversible, no hay transferencia de energía como calor porque el proceso es adiabático; δQ = 0. Por el contrario, si el proceso es irreversible, se produce entropía dentro del sistema; en consecuencia, para mantener constante la entropía dentro del sistema, debe eliminarse simultáneamente energía del sistema en forma de calor.
Para los procesos reversibles, se realiza una transformación isentrópica "aislando" térmicamente el sistema de su entorno. La temperatura es la variable conjugada termodinámica a la entropía, por lo que el proceso conjugado sería un proceso isotérmico, en el que el sistema está "conectado" térmicamente a un baño de calor de temperatura constante.
Procesos isentrópicos en sistemas termodinámicos[editar]
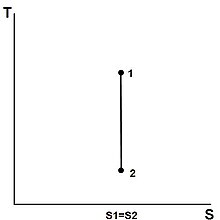
La entropía de una masa dada no cambia durante un proceso que es internamente reversible y adiabático. Un proceso durante el cual la entropía permanece constante se denomina proceso isentrópico, escrito o .[13]. Algunos ejemplos de dispositivos termodinámicos teóricamente isentrópicos son las bombas, los compresores de gas, las turbinas, las toberas y los difusores.
Eficiencias isentrópicas de los dispositivos de flujo constante en sistemas termodinámicos[editar]
La mayoría de los dispositivos de flujo constante funcionan en condiciones adiabáticas, y el proceso ideal para estos dispositivos es el proceso isentrópico. El parámetro que describe la eficiencia con la que un dispositivo se aproxima a un dispositivo isentrópico correspondiente se denomina eficiencia isentrópica o adiabática.[13]
Eficiencia isentrópica de las turbinas:
Rendimiento isentrópico de los compresores:
Eficiencia isentrópica de las toberas:
Para todas las ecuaciones anteriores:
- es la entalpía específica en el estado de entrada,
- es la entalpía específica en el estado de salida para el proceso real,
- es la entalpía específica en el estado de salida para el proceso isentrópico.
Dispositivos isentrópicos en ciclos termodinámicos[editar]
Referencias[editar]
- ↑ Partington, J. R. (1949), An Advanced Treatise on Physical Chemistry. 1, Fundamental Principles. The Properties of Gases, London: Longmans, Green and Co., p. 122..
- ↑ Kestin, J. (1966). A Course in Thermodynamics, Blaisdell Publishing Company, Waltham MA, p. 196.
- ↑ Münster, A. (1970). Classical Thermodynamics, translated by E. S. Halberstadt, Wiley–Interscience, London, ISBN 0-471-62430-6, p. 13.
- ↑ Haase, R. (1971). Survey of Fundamental Laws, chapter 1 of Thermodynamics, pages 1–97 of volume 1, ed. W. Jost, of Physical Chemistry. An Advanced Treatise, ed. H. Eyring, D. Henderson, W. Jost, Academic Press, New York, lcn 73–117081, p. 71.
- ↑ Borgnakke, C., Sonntag., R.E. (2009). Fundamentals of Thermodynamics, seventh edition, Wiley, ISBN 978-0-470-04192-5, p. 310.
- ↑ Massey, B. S. (1970), Mechanics of Fluids, Section 12.2 (2nd edition) Van Nostrand Reinhold Company, London. Library of Congress Catalog Card Number: 67-25005, p. 19.
- ↑ Çengel, Y. A., Boles, M. A. (2015). Thermodynamics: An Engineering Approach, 8th edition, McGraw-Hill, New York, ISBN 978-0-07-339817-4, p. 340.
- ↑ Çengel, Y. A., Boles, M. A. (2015). Termodinámica: An Engineering Approach, 8ª edición, McGraw-Hill, Nueva York, ISBN 978-0-07-339817-4, pp. 340-341.
- ↑ Mortimer, R. G. Physical Chemistry, 3rd ed., p. 120, Academic Press, 2008.
- ↑ Fermi, E. Thermodynamics, footnote on p. 48, Dover Publications,1956 (still in print).
- ↑ Guggenheim, E. A. (1985). Thermodynamics. An Advanced Treatment for Chemists and Physicists, séptima edición, North Holland, Amsterdam, ISBN 0444869514, p. 12: "Como caso límite entre los procesos naturales y no naturales[,] tenemos los procesos reversibles, que consisten en el paso en cualquier dirección a través de una serie continua de estados de equilibrio. Los procesos reversibles no ocurren realmente..."
- ↑ Kestin, J. (1966). A Course in Thermodynamics, Blaisdell Publishing Company, Waltham MA, p. 127: "Sin embargo, por un tramo de imaginación, se aceptó que un proceso, la compresión o la expansión, según se desee, podría realizarse "infinitamente lento"[,] o como se dice a veces, "cuasistáticamente"." P. 130: "Está claro que todos los procesos naturales son irreversibles y que los procesos reversibles constituyen sólo idealizaciones convenientes."
- ↑ a b Cengel, Yunus A., y Michaeul A. Boles. Thermodynamics: An Engineering Approach. 7th Edition ed. New York: Mcgraw-Hill, 2012















